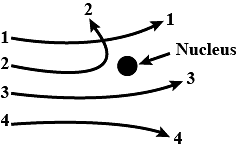
α- ಕಣದ ಪ್ರಕ್ಷೇಪ ಪಥ
ಭೌತಶಾಸ್ತ್ರ
α- ಕಣದ ಹೀಲಿಯಮ್ ಪರಮಾಣುಗಳ ನ್ಯೂಕ್ಲಿಯಸ್ಗಳಾಗಿದ್ದು 2e ಪ್ರಮಾಣದ ಧನ ವಿದ್ಯುದಾವೇಶ ಮತ್ತು ಹೀಲಿಯಮ್ ಪರಮಾಣುವಿನ ರಾಶಿಯನ್ನು ಹೊಂದಿವೆ. ನ್ಯೂಟನ್ ಚಲನೆಯ ಎರಡನೇ ನಿಯಮ ಮತ್ತು ಕೊಲೂಂಬ್ ಸ್ಥಾಯೀ ವಿದ್ಯುದಾವೇಶ ವಿಕರ್ಷಣ ಬಲದ ನಿಯಮದ ಪ್ರಕಾರ, ನ್ಯೂಕ್ಲಿಯಸ್ ಮತ್ತು α- ಕಣದ ನಡುವಿನ ವಿಕರ್ಷಣ ಬಲವು,
α- ಕಣ ಮತ್ತು ನ್ಯೂಕ್ಲಿಯಸ್ ನಡುವಿನ ಅಂತರ, α- ಕಣದ ಪ್ರಕ್ಷೇಪ ಪಥವು ಸಂಘಟನೆಯ ತಾಡಣ ಚರ b ಯ ಮೇಲೆ ಅವಲಂಬಿತವಾಗಿರುತ್ತದೆ. ತಾಡಣ ಚರ ಕನಿಷ್ಠವಾಗಿದ್ದಾಗ α- ಕಣಗಳು ಹಿಂಪುಟಿಯುತ್ತವೆ. ತಾಡಣ ಚರ ದೂರವಿದ್ದಾಗ α- ಕಣಗಳು ಕಡಿಮೆ ವಿಚಲಿತವಾಗುತ್ತವೆ.
ಎಲೆಕ್ಟ್ರಾನ್ ಕಕ್ಷೆಗಳು
ಎಲೆಕ್ಟ್ರಾನ್ಗಳು ಸ್ಥಾಯೀ ವಿದ್ಯುತ್ ಬಲ (fe)ದಿಂದ ಪಡೆದ ಕೇಂದ್ರಾಭಿಮುಖ ಬಲ (fc) ವನ್ನು ಪಡೆಯುವುದರಿಂದ ಸ್ಥಿರ ಕಕ್ಷೆಯಾಗಿ fe= fc ಇರಬೇಕಾಗುತ್ತದೆ.ಎಲೆಕ್ಟ್ರಾನ್ಗಳು ಋಣ ಶಕ್ತಿಯು ನ್ಯೂಕ್ಲಿಯಸ್ಗೆ ಬಂಧಿತವಾಗಿದೆ ಎಂದು ಸೂಚಿಸುತ್ತವೆ.
ಪರಮಾಣುವಿನ ರೋಹಿತಗಳು
ಕಡಿಮೆ ಒತ್ತಡದಲ್ಲಿ ಅನಿಲ ಅಥವಾ ಆವಿಯ ಮೂಲಕ ವಿದ್ಯುತ್ ಅನ್ನು ಸಾಮಾನ್ಯವಾಗಿ ಹರಿಸಿದಾಗ ಅದು ಉತ್ತೇಜನಗೊಂಡು ಹೊರಸೂಸುವ ವಿಶೇಷವಾದ ನಿರ್ದಿಷ್ಟ ತರಂಗಾಂತರಗಳ ರೋಹಿತವನ್ನು ‘ಉತ್ಸರ್ಜನಾ ರೇಖಾ ರೋಹಿತ’ ಎಂದು ಕರೆಯುತ್ತಾರೆ. ಇದು ಪ್ರತೀ ದ್ಯವ್ಯಕ್ಕೂ ವಿಭಿನ್ನವಾಗಿದ್ದು, ಇದನ್ನು ಬೆರಳಚ್ಚಿನಂತೆ ಉಪಯೋಗಿಸುತ್ತಾರೆ.
ರೋಹಿತ ಶ್ರೇಣಿಗಳು
ಜಾನ್ ಜೇಕಬ್ ಬಾಮರ್ ಅವರು ಹೈಡ್ರೋಜನ್ ರೋಹಿತ ಶ್ರೇಣಿಯನ್ನು ಮೊದಲು ಗೋಚರ ವಲಯದಲ್ಲಿ ವಿಶ್ಲೇಷಿಸಿದರು. ಈ ಶ್ರೇಣಿಯನ್ನು ಬಾಮರ್ ಶ್ರೇಣಿ ಎನ್ನುವರು.
ಕೆಂಬಣ್ಣದ ಅತಿ ಉದ್ದ ತರಂಗಾಂತರ 656.3 nm ಹೊಂದಿರುವ ಗೆರೆಯನ್ನು H α ಎಂದು, ತದನಂತರ ನೀಲಿ ಹಸಿರು ಇರುವ ಬಣ್ಣದ ತರಂಗಾಂತರ 486.1 nm ಹೊಂದಿರುವ ಗೆರೆಯನ್ನು H α, ನೇರಳೆ ಬಣ್ಣದ ತರಂಗಾಂತರ 434.1 nm ಹೊಂದಿರುವ ರೇಖೆಯನ್ನು H r ಎಂದು ಕರೆಯುತ್ತಾರೆ. ತರಂಗಾಂತರ ಕಡಿಮೆಯಾಗುತ್ತಾ ಹೋದಂತೆ ಗೆರೆಗಳು ಹತ್ತಿರವಾಗುತ್ತಾ ಹೋಗುತ್ತವೆ.
ತಾಜಾ ಸುದ್ದಿಗಾಗಿ ಪ್ರಜಾವಾಣಿ ಟೆಲಿಗ್ರಾಂ ಚಾನೆಲ್ ಸೇರಿಕೊಳ್ಳಿ | ಪ್ರಜಾವಾಣಿ ಆ್ಯಪ್ ಇಲ್ಲಿದೆ: ಆಂಡ್ರಾಯ್ಡ್ | ಐಒಎಸ್ | ನಮ್ಮ ಫೇಸ್ಬುಕ್ ಪುಟ ಫಾಲೋ ಮಾಡಿ.

